
沙格医疗已成功帮助多家医疗器械制造商获得8张澳洲TGA证书,涉及I类,I类灭菌,IIa类等不同类别的产品。最短仅历时四天下证!



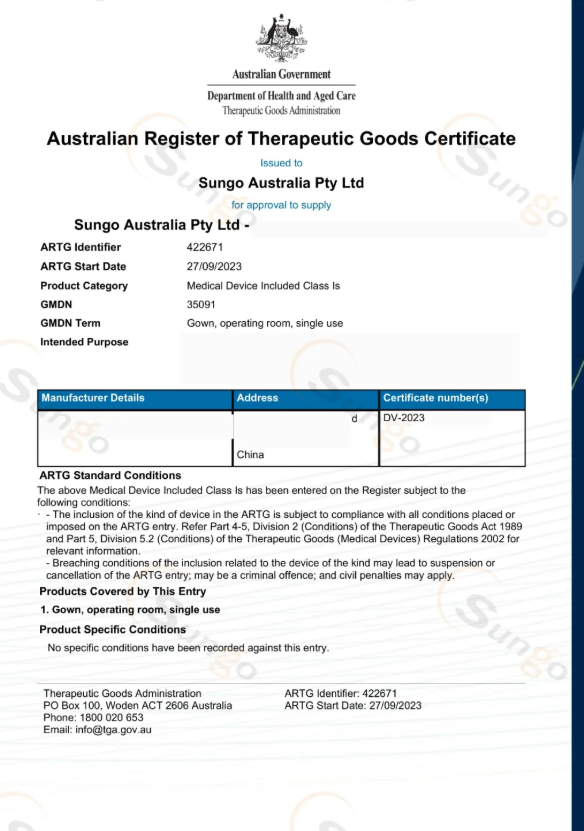
什么是澳洲TGA证书?
根据《澳大利亚医疗用品法》(1989年)规定,所有在澳大利亚上市的医疗用品必须按有关要求,向TGA提出注册或登记申请,获得注册登记(Australian Register of Therapeutic Goods,ARTG)后才能合法上市。
澳大利亚是世界上公认的医疗用品管理最严格、市场准入标准最高的国家之一。
澳洲医疗器械是如何分类的?
澳⼤利亚医疗器械的分类是根据⻛险归类的,原则上⽐较贴近欧盟的MDR/IVDR法规。
器械出口澳洲是否需要在当地委派授权代表?
器械制造商必须委派一名澳洲代理人(Sponsor)负责医疗器械进出口以及和医疗器械相关的合规活动;Sponsor必须确保申报器械的安全有效性,并持续承担器械的上市后安全责任;
风险等级较高的器械难点有哪些?
相对于普通I类产品而言,更高风险等级的产品在申请ARTG注册之前要求通过澳洲公告机构的认证。澳洲认证的时间较长,复杂程度较高。
若制造商有其他国家的审批文件,可以作为作为澳洲符合性评估文件,从而大大缩短审批时间,节省了申报成本。
澳洲认可哪些国家的审批文件?
- 欧盟公告机构根据MDD,IVDD指令,MDR或IVDR法规颁发的CE证书;
- 美国FDA颁发的510K Summary;
- 加拿大健康部颁发的MDL证书;
- 日本厚生劳动省(MHLW),日本药品和医疗器械管理局(PMDA)或注册认证机构(RCB)的器械上市前批准;
- 新加坡卫生科学管理局(HSA)注册函;
- 纳入澳洲医疗器械法规的MDSAP证书;
- IAF认可机构颁发的13485证书;
SUNGO优势














