
【510K】中国企业首获灭菌指示胶带510(K) K号!
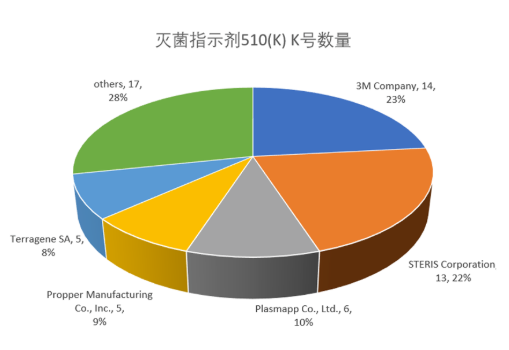
长期以来,美国市场灭菌指示物被3M、STERIS等国际大公司所垄断,造成这种状态的主要原因是灭菌指示物按美国法规要求,检测难度较大,FDA申报困难,许多国内公司望而却步。
2024年12月,沙格公司成功协助国内一家灭菌指示胶带生产企业获得中国 EO、湿热灭菌指示胶带的510(K) K号。
在此次申报过程中,沙格公司的咨询团队与检测团队紧密合作,针对客户产品定位于EO和湿热灭菌指示特性,量身定制了灭菌指示胶带检测方案。我们在测试前与客户逐一核对,确保所有流程合规。样品到达后,实验室高效执行检测,为客户顺利获得K号奠定了坚实基础。
灭菌指示胶带510K申报,检测内容主要包括:
灭菌验证:使用美国上市的EO和湿热灭菌器进行指示胶带灭菌验证
货架寿命评估
ISO 11140-1指示剂性能检测
灭菌后稳定性研究
生物学评估或测试
沙格集团聚焦于检验检测服务的技术平台,经过了两年多的发展,目前已经建成了上海实验室、合肥实验室两个检测实验场地,可为客户进行手术衣、隔离衣、医用手套、医用口罩等性能检测,轮椅车、代步车、拐杖、助行器等康复医疗器械性能检测、包装验证和模拟运输等无菌医疗器械产品包装通用检测,所出具的检测报告已获美国、欧盟、英国等全球主要医疗器械国际市场的主管当局认可。














